|
Femarelle® (DT56a)
Symptômes de la ménopause et Femarelle® La santé osseuse : Les études La santé vaginale* ➠ Étude clinique: Atrophie vaginale*Santé Canada n’a pas approuvé Femarelle pour le traitement de l’atrophie vaginale; l’utiliser à cette fin serait considéré comme une utilisation hors indication.La thrombogénicité Cancer du sein* ➠ Étude préclinique de sécurité : Tissu de cancer du sein chez l'humain*L’utilisation de Femarelle n’est pas recommandée chez les patientes avec un cancer du sein.La toxicologie Résumé |
Étude clinique: Atrophie vaginaleA Prospective Study of DT56a (Femarelle®) for the treatment of Postmenopausal Vaginal Atrophy. Nachtigall M et al. Menopause book of abstracts of the NAMS 22nd Annual Meeting Sept 2011 (Article in process)L’atrophie vaginale est due à de bas taux d’œstrogènes sur une période prolongée et affecte de 10 à 40 % des femmes postménopausées. Elle peut se manifester par une douleur, une sècheresse, un prurit, une dyspareunie ou des saignements vaginaux lors de contacts. Contrairement aux symptômes comme les bouffées de chaleur, l’atrophie vaginale ne diminue pas au fil du temps et sa gravité progresse souvent.
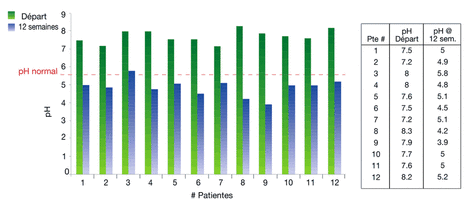
Pour étudier l’effet de Femarelle® sur l’atrophie vaginale, 12 femmes postménopausées atteintes d’atrophie vaginale (< 5 % de cellules superficielles à la cytologie cervicale) avec au moins un symptôme modéré à grave (sècheresse - 2, irritation - 1, douleur - 3, dysurie - 0, dyspareunie - 5, saignements lors du coït - 1) ont été recrutées pour une étude pilote ouverte de 12 semaines. Les capsules de Femarelle® ont été données 2 fois par jour pendant 12 semaines. Lors de chaque visite (0, 4 et 12 semaines), les sujets ont passé une évaluation pour l’atrophie vaginale (examen au spéculum, indice de maturation, pH vaginal) et rempli des questionnaires sur leurs symptômes d’atrophie et leur qualité de vie (Utian Quality of Life - UQoL). Des examens physiques, des tests Pap, des cultures vaginales et des analyses sanguines ont également été effectués aux semaines 0 et 12. Résultats : Les 12 patientes, qui étaient extrêmement atrophiques, ont fait état d’une amélioration significative de leur symptôme le plus préoccupant. Chez toutes les femmes, une diminution significative du pH vaginal a été mesurée à partir de la valeur de référence de 7,7 ± 2,2, passant à 4,9 ± 1,4 à la semaine 12 (p < 0,0001). (Figure 10) Une amélioration significative a également été constatée pour l’indice de maturation. Le taux de cellules parabasales, qui était de 100 % au départ, était de 43 % après 12 semaines de traitement. Le taux de cellules intermédiaires est passé de 0 à 47 % et le taux de cellules superficielles, qui était de 0 % au départ, était de 10 % après 12 semaines de traitement avec du Femarelle®. Toutes ces données étaient statistiquement significatives, p < 0,001. Une amélioration significative a été constatée pour l’indice UQoL, celui-ci passant d’une moyenne pré-traitement de 75,4 ± 22,7 points à une moyenne post-traitement de 88,9 ± 26,8 (p < 0,001). On a noté une amélioration significative dans la section Sexualité de l’UQoL, le score passant de 6,5 ± 2 points (moyenne pré-traitement) à 10,6 ± 3,2 (moyenne post-traitement) (p < 0,001) |
Conclusion : Femarelle® est une bonne option pour une utilisation à long terme pendant et après la ménopause; il fournit à la fois un soulagement des symptômes vasomoteurs chez la femme commençant sa ménopause et un soulagement de l’atrophie vaginale chez la femme postménopausée, même dans des conditions très atrophiques.6
Santé Canada n’a pas approuvé Femarelle® pour le traitement de l’atrophie vaginale; l’utiliser à cette fin serait considéré comme une utilisation hors indication.
Étude clinique : Coagulation du sang
The Selective Estrogen Receptor Modulator (SERM) DT56a (Femarelle) does not affect platelet reactivity in normal or thrombophilic menopausal women. Nachtigall L. et al. Menopause 2009
L’hormonothérapie et l’œstrogénothérapie augmentent la formation de caillots sanguins, ce qui peut conduire à une thromboembolie veineuse (TEV) et à un AVC; elles ne peuvent donc pas être données aux femmes ayant un temps de coagulation raccourci.
Il est estimé que l’incidence du facteur V Leiden hérité et de d’autres facteurs de risque de TEV dans la population générale se situe entre 5 et 10 %. Cette population est exposée à un risque de développer une TEV de 5 à 21 fois plus élevé.
Pour étudier l’effet de Femarelle® sur le système de coagulation, un dispositif d’évaluation de l’adhésion et de l’agrégation plaquettaires (PFA-100) a été utilisé. Le PFA-100 mesure le temps requis pour que du sang aspiré dans un fin capillaire bloque une membrane enduite de collagène et d’épinéphrine (CEPI) ou de collagène et d’ADP (CADP). Ce temps est appelé le temps de fermeture (TF) et est mesuré en secondes pour évaluer le temps de coagulation du sang en circulation. La mesure du temps de fermeture du PFA-100 est considérée comme égale au temps de coagulation lors d’évaluation de la coagulation et de l’adhésion plaquettaires, ainsi que des facteurs d’agrégation et de coagulation sanguine.
L’analyseur de la fonction plaquettaire PFA-100 a été utilisé pour évaluer la réactivité des plaquettes au départ et après huit semaines de traitement par Femarelle® chez 25 femmes postménopausées symptomatiques ayant des temps de coagulation normaux et sept femmes symptomatiques ayant des temps de coagulation raccourcis (< 61 secondes). Les temps de fermeture ont été mesurés après 3 semaines et 8 semaines chez tous les sujets et après un an chez les femmes ayant des temps de coagulation raccourcis.
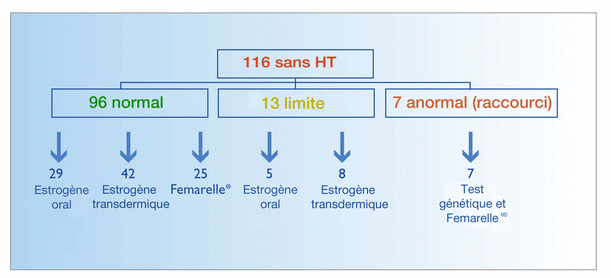
Un total de 116 femmes postménopausées symptomatiques ont été analysées avec le dispositif PFA-100 dans deux essais cliniques différents. (Figure 16)
Un total de 96 femmes se sont avérées avoir des temps de coagulation normaux (CEPI 85 à 165 secondes et CADP 71 à 118 secondes). De ce groupe, 29 femmes ont pris des œstrogènes par voie orale, 42 femmes ont pris des œstrogènes par voie transdermique et 25 femmes ayant des temps de coagulation normaux ont été traitées par Femarelle® pendant 8 semaines.
13 femmes avaient des temps limites de coagulation (CEPI 70-84 et CADP 56-70 sec.); 5 femmes ont été traitées avec des estrogènes oraux et 8 femmes avec des estrogènes transdermiques pendant 8 semaines.
Sept femmes ayant des temps de fermeture courts (< 61 secondes) ont été exclues pour un traitement d’hormonothérapie et ont passé un examen complet de la thrombophilie. Ces femmes ont ensuite été traitées par Femarelle®. Les temps de fermeture ont été mesurés après 3 semaines, 8 semaines et un an de traitement.
Il est estimé que l’incidence du facteur V Leiden hérité et de d’autres facteurs de risque de TEV dans la population générale se situe entre 5 et 10 %. Cette population est exposée à un risque de développer une TEV de 5 à 21 fois plus élevé.
Pour étudier l’effet de Femarelle® sur le système de coagulation, un dispositif d’évaluation de l’adhésion et de l’agrégation plaquettaires (PFA-100) a été utilisé. Le PFA-100 mesure le temps requis pour que du sang aspiré dans un fin capillaire bloque une membrane enduite de collagène et d’épinéphrine (CEPI) ou de collagène et d’ADP (CADP). Ce temps est appelé le temps de fermeture (TF) et est mesuré en secondes pour évaluer le temps de coagulation du sang en circulation. La mesure du temps de fermeture du PFA-100 est considérée comme égale au temps de coagulation lors d’évaluation de la coagulation et de l’adhésion plaquettaires, ainsi que des facteurs d’agrégation et de coagulation sanguine.
L’analyseur de la fonction plaquettaire PFA-100 a été utilisé pour évaluer la réactivité des plaquettes au départ et après huit semaines de traitement par Femarelle® chez 25 femmes postménopausées symptomatiques ayant des temps de coagulation normaux et sept femmes symptomatiques ayant des temps de coagulation raccourcis (< 61 secondes). Les temps de fermeture ont été mesurés après 3 semaines et 8 semaines chez tous les sujets et après un an chez les femmes ayant des temps de coagulation raccourcis.
Un total de 116 femmes postménopausées symptomatiques ont été analysées avec le dispositif PFA-100 dans deux essais cliniques différents. (Figure 16)
Un total de 96 femmes se sont avérées avoir des temps de coagulation normaux (CEPI 85 à 165 secondes et CADP 71 à 118 secondes). De ce groupe, 29 femmes ont pris des œstrogènes par voie orale, 42 femmes ont pris des œstrogènes par voie transdermique et 25 femmes ayant des temps de coagulation normaux ont été traitées par Femarelle® pendant 8 semaines.
13 femmes avaient des temps limites de coagulation (CEPI 70-84 et CADP 56-70 sec.); 5 femmes ont été traitées avec des estrogènes oraux et 8 femmes avec des estrogènes transdermiques pendant 8 semaines.
Sept femmes ayant des temps de fermeture courts (< 61 secondes) ont été exclues pour un traitement d’hormonothérapie et ont passé un examen complet de la thrombophilie. Ces femmes ont ensuite été traitées par Femarelle®. Les temps de fermeture ont été mesurés après 3 semaines, 8 semaines et un an de traitement.
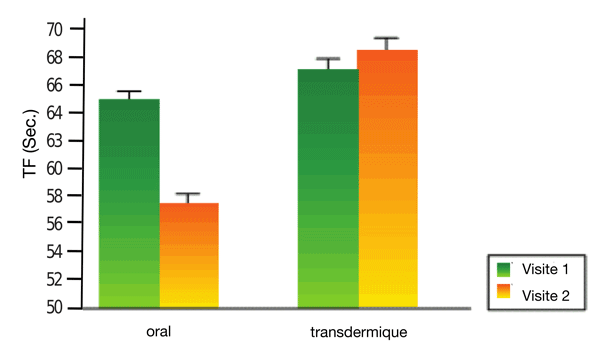
Résultats : Il a été constaté que les femmes ayant un temps de coagulation normal et ayant pris soit des œstrogènes par voie orale soit des œstrogènes par voie transdermique ne présentaient aucun changement du TF après 8 semaines de traitement. Cependant, les femmes dont le temps de coagulation était limite qui ont été traitées avec des œstrogènes par voie orale ont présenté une diminution significative du temps de coagulation, tandis que celles traitées avec des œstrogènes par voie transdermique ne présentaient aucun changement du TF13 (figure 17)
|
Figure 17 Temps de fermeture CADP avec des œstrogènes par voie orale ou transdermique chez les femmes ayant des temps de coagulation limites
Les femmes du groupe recevant Femarelle® et ayant un temps de coagulation normal (n = 25) ne présentaient aucun changement du temps de coagulation après avoir pris Femarelle® pendant de trois à huit semaines.
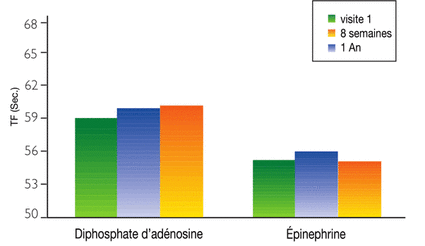
Les sept femmes ayant des temps de fermeture plus courts (CEPI ÷ 60 secondes et CADP ÷ 56 secondes) ont confirmé les anomalies associées à une thrombophilie (tableau 3). Aucune modification significative des temps de fermeture n’a été observée dans ce groupe après trois semaines, huit semaines ou une année de traitement par Femarelle® (figure 18) |
Conclusion : Les études évaluant l’incidence de la TEV chez les femmes prenant une hormonothérapie signalent que la plus grande augmentation absolue de l’incidence de TEV a lieu peu de temps après le début du traitement.14 Le fait qu’un traitement d’un an par Femarelle® n’a aucunement modifié les temps de coagulation des sept femmes thrombophiliques souligne l’innocuité du produit en ce qui concerne la fonction plaquettaire. Femarelle® offre donc un nouveau choix clinique pour le traitement des symptômes de la ménopause sans thrombogénicité.15
Étude préclinique de sécurité : Tissu de cancer du sein chez l'humain
Pharmacological Doses of the Natural phyto-SERM DT56a (Femarelle) Have no Effect on MCF-7 Breast Cancer Cell-Line. Yoles I., and Lilling G. European J. of Obstetrics & Gynecology & Reproductive Biology 2006
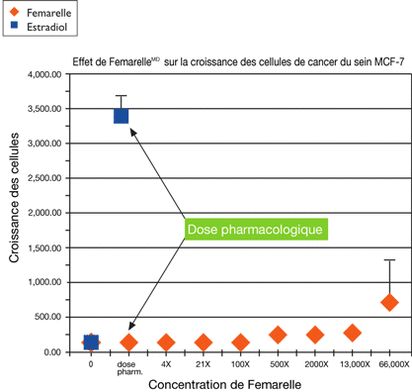
Les tumeurs positives pour les œstrogènes représentent 70 % de tous les cas de cancer du sein.21 Un modèle commun pour examiner l’activité œstrogénique des composés passe par l’utilisation des cellules de la lignée de cancer du sein MCF-7. Les cellules MCF-7 sont des cellules de cancer du sein qui dépendent des œstrogènes.
Une étude a été menée sur cette lignée cellulaire afin de déterminer si Femarelle® (DT56a) a un quelconque effet œstrogénique sur le tissu mammaire.
Les cellules MCF-7 ont été ensemencées et incubées pendant 96 heures dans un milieu appauvri en œstrogènes et ont ensuite été incubées avec Femarelle® ou E2 pendant 72 heures. La dose pharmacologique pour E2 a été ajoutée aux cellules en culture. Femarelle® a été ajouté en doses fractionnées commençant à la dose pharmacologique calculée et montant jusqu’à 66 000 fois la dose pharmacologique.
Resultats : Contrairement à E2, Femarelle® n’a pas stimulé les récepteurs des œstrogènes dans les tissus mammaires et n’a donc pas induit la prolifération des cellules cancéreuses (figure 15)
Une étude a été menée sur cette lignée cellulaire afin de déterminer si Femarelle® (DT56a) a un quelconque effet œstrogénique sur le tissu mammaire.
Les cellules MCF-7 ont été ensemencées et incubées pendant 96 heures dans un milieu appauvri en œstrogènes et ont ensuite été incubées avec Femarelle® ou E2 pendant 72 heures. La dose pharmacologique pour E2 a été ajoutée aux cellules en culture. Femarelle® a été ajouté en doses fractionnées commençant à la dose pharmacologique calculée et montant jusqu’à 66 000 fois la dose pharmacologique.
Resultats : Contrairement à E2, Femarelle® n’a pas stimulé les récepteurs des œstrogènes dans les tissus mammaires et n’a donc pas induit la prolifération des cellules cancéreuses (figure 15)
Une augmentation significative de l’activité de la CK a été constatée après le traitement par E2 et Femarelle® dans les tissus squelettiques (épiphyse et diaphyse). Cependant, alors que E2 a produit une importante activation de la CK dans l’utérus, Femarelle® n’a eu aucun effet stimulant sur ce site.
Conclusion: Femarelle® ne déclenche pas la croissance des cellules de cancer du sein. Cette découverte soutient également les données vérifiant l’activité de Femarelle® en tant que MSRO.12
L’utilisation de Femarelle® n’est pas recommandée chez les patientes avec un cancer du sein.
Étude préclinique : Toxicologie
Femarelle lacks peripheral estrogen-like actions in the rat reproductive tract. Oropeza M.V. Orozco S., Ponce H., Campos M.G. Reproductive Toxicology 2005
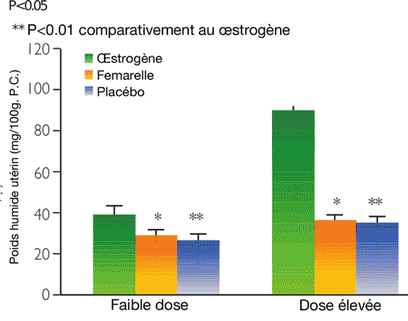
Une étude de toxicité n’a pas réussi à démontrer d’effets secondaires œstrogéniques de Femarelle® sur les caractéristiques dépendantes aux œstrogènes de l’appareil reproducteur féminin dans un modèle postménopausées de rates OVX. Dans cette étude, des rates OVX adultes ont été traitées de manière aléatoire pendant 14 jours avec un placébo ou avec une faible ou une forte dose d’E2 ou de Femarelle®. La faible dose a été calculée comme étant 3 fois la dose recommandée (DR) alors que la dose élevée était égale à 9 fois la DR.
Le poids de l’utérus, la kératinisation de la muqueuse vaginale et la sensibilité du muscle lisse de l’utérus à la sérotonine ont été surveillés.
Résultats : À la différence d’E2, Femarelle® ne présentait aucun effet œstrogénique sur le poids de l’utérus (figure 20) et aucune sensibilité à la sérotonine (figure 21). Par rapport aux rates traitées avec E2, la muqueuse vaginale des rates traitées par Femarelle® présentait un faible degré de kératinisation.
Le poids de l’utérus, la kératinisation de la muqueuse vaginale et la sensibilité du muscle lisse de l’utérus à la sérotonine ont été surveillés.
Résultats : À la différence d’E2, Femarelle® ne présentait aucun effet œstrogénique sur le poids de l’utérus (figure 20) et aucune sensibilité à la sérotonine (figure 21). Par rapport aux rates traitées avec E2, la muqueuse vaginale des rates traitées par Femarelle® présentait un faible degré de kératinisation.
|
Figure 20 : Poids humide de l’utérus de rates OVX traitées avec une dose faible ou élevée d’œstrogènes conjugués d’origine équine et de Femarelle®
|
Figure 21 : Traces polygraphiques de l’activité contractile de segments utérins provenant de rates OVX traitées avec une dose faible ou élevée d’estrogènes conjugués d’origine équine, E2 et de Femarelle®
|
Conclusion : Les résultats ci-dessus révèlent que Femarelle® n’a pas d’effets œstrogéniques sur l’utérus.17
Femarelle® en tant que MSRO
Sommaire des études mentionnées dans notre site internet et dans le document de Besins, intitulé Revue des données cliniques.
Les données cliniques et précliniques présentées dans cette monographie ont indiqué que Femarelle® agit comme un nouveau modulateur sélectif des récepteurs des œstrogènes (MSRO) qui affecte les récepteurs des œstrogènes seulement au niveau de sites spécifiques sans affecter les tissus où un quelconque changement peut avoir des conséquences dangereuses.
Femarelle® pris deux fois par jour (matin et soir) est efficace pour le soulagement des symptômes de la ménopause et soutenir la santé osseuse. La recherche et l’expérience clinique ont montré que le soulagement des symptômes de la ménopause est ressenti, en moyenne, au cours du premier mois de traitement. Trois femmes sur quatre signalent un soulagement, avec une réduction des bouffées de chaleur dans 76 % des cas, un soulagement des douleurs articulaires et musculaires dans 70 % des cas et un soulagement des maux de tête dans 68 % des cas (ceux-ci étant les principaux symptômes associés à la transition de la ménopause). Ces taux étaient statistiquement significatifs (p < 0,01).4, 7, 19
Femarelle® s’est avéré être efficace pour l’atrophie vulvo-vaginale, une condition signalée par 75 % des femmes postménopausées.6 D’autres études cliniques sont nécessaires pour mieux comprendre l’impact de Femarelle® sur la santé vaginale des femmes postménopausées. Santé Canada n’a pas approuvé l’utilisation de Femarelle® pour le traitement des problèmes de santé vulvo-vaginaux.
L’effet de Femarelle® sur les os a démontré une augmentation statistiquement significative de 2,0 % de la DMO dans la hanche et de 3,6 % dans la colonne vertébrale après 12 mois de traitement. L’effet positif de Femarelle® sur les os a également été démontré dans des modèles animaux.7, 11 Femarelle® soutient la santé osseuse des femmes postménopausées.
Ces résultats cliniques ont été obtenus sans provoquer de changements dans les paramètres de coagulation ou le profil hormonal sanguin et sans causer de modification de l’épaisseur de l’endomètre ou d’autres changements dans l’utérus.4, 7, 9, 15, 18, 19
Une étude de son mécanisme d’action sur la DMO dans des cultures d’os humains a révélé que Femarelle® présente des propriétés de formation osseuse uniques en augmentant la formation osseuse par l’intermédiaire de l’activité des ostéoblastes tout en entravant le développement des cellules adipeuses dans la moelle osseuse, induisant ainsi le rajeunissement de l’os.10, 11 Comme Femarelle® agit différemment d’E2 dans un environnement à haute teneur en glucose, il peut être un agent de restauration des os efficace chez les femmes diabétiques postménopausées, ce qui pourrait aider à maintenir la santé osseuse.16
Femarelle® n’a eu aucun effet sur les tissus cancéreux dans une étude avec une culture de tissu de cancer du sein humain.12 L’utilisation de Femarelle n’est pas recommandée pour les patientes avec un cancer du sein.
L’effet positif de Femarelle® sur la neurostéroïdogénèse du cerveau et le système opioïdergique peut expliquer en partie l’effet clinique de Femarelle® sur les symptômes de la ménopause.5
Le complexe actif unique contenu dans Femarelle® représente un traitement nouveau et efficace. Il n’existe pas d’autres traitements chimiquement semblables pour l’usage humain. Le mécanisme d’action sélectif de Femarelle® lui permet d’agir comme un agoniste sur les récepteurs des œstrogènes et donc d’exercer un effet favorable sur les symptômes de la ménopause (bouffées de chaleur et les troubles du sommeil) et la DMO pour aider à la santé osseuse alors qu’il a un effet antagoniste sur les récepteurs oestrogéniques dans les tissus du sein et de l’utérus.
L’efficacité de Femarelle® s’est avérée être similaire à l’efficacité de l’hormonothérapie, mais en raison de ses propriétés sélectives, Femarelle® fournit une solution plus sécuritaire pour la prise en charge à long terme de la ménopause.19
Femarelle® est donc, pour toutes ces raisons, une thérapie de première ligne appropriée, sécuritaire et efficace pour le traitement des symptômes de la ménopause et pour soutenir la santé osseuse.
Femarelle® pris deux fois par jour (matin et soir) est efficace pour le soulagement des symptômes de la ménopause et soutenir la santé osseuse. La recherche et l’expérience clinique ont montré que le soulagement des symptômes de la ménopause est ressenti, en moyenne, au cours du premier mois de traitement. Trois femmes sur quatre signalent un soulagement, avec une réduction des bouffées de chaleur dans 76 % des cas, un soulagement des douleurs articulaires et musculaires dans 70 % des cas et un soulagement des maux de tête dans 68 % des cas (ceux-ci étant les principaux symptômes associés à la transition de la ménopause). Ces taux étaient statistiquement significatifs (p < 0,01).4, 7, 19
Femarelle® s’est avéré être efficace pour l’atrophie vulvo-vaginale, une condition signalée par 75 % des femmes postménopausées.6 D’autres études cliniques sont nécessaires pour mieux comprendre l’impact de Femarelle® sur la santé vaginale des femmes postménopausées. Santé Canada n’a pas approuvé l’utilisation de Femarelle® pour le traitement des problèmes de santé vulvo-vaginaux.
L’effet de Femarelle® sur les os a démontré une augmentation statistiquement significative de 2,0 % de la DMO dans la hanche et de 3,6 % dans la colonne vertébrale après 12 mois de traitement. L’effet positif de Femarelle® sur les os a également été démontré dans des modèles animaux.7, 11 Femarelle® soutient la santé osseuse des femmes postménopausées.
Ces résultats cliniques ont été obtenus sans provoquer de changements dans les paramètres de coagulation ou le profil hormonal sanguin et sans causer de modification de l’épaisseur de l’endomètre ou d’autres changements dans l’utérus.4, 7, 9, 15, 18, 19
Une étude de son mécanisme d’action sur la DMO dans des cultures d’os humains a révélé que Femarelle® présente des propriétés de formation osseuse uniques en augmentant la formation osseuse par l’intermédiaire de l’activité des ostéoblastes tout en entravant le développement des cellules adipeuses dans la moelle osseuse, induisant ainsi le rajeunissement de l’os.10, 11 Comme Femarelle® agit différemment d’E2 dans un environnement à haute teneur en glucose, il peut être un agent de restauration des os efficace chez les femmes diabétiques postménopausées, ce qui pourrait aider à maintenir la santé osseuse.16
Femarelle® n’a eu aucun effet sur les tissus cancéreux dans une étude avec une culture de tissu de cancer du sein humain.12 L’utilisation de Femarelle n’est pas recommandée pour les patientes avec un cancer du sein.
L’effet positif de Femarelle® sur la neurostéroïdogénèse du cerveau et le système opioïdergique peut expliquer en partie l’effet clinique de Femarelle® sur les symptômes de la ménopause.5
Le complexe actif unique contenu dans Femarelle® représente un traitement nouveau et efficace. Il n’existe pas d’autres traitements chimiquement semblables pour l’usage humain. Le mécanisme d’action sélectif de Femarelle® lui permet d’agir comme un agoniste sur les récepteurs des œstrogènes et donc d’exercer un effet favorable sur les symptômes de la ménopause (bouffées de chaleur et les troubles du sommeil) et la DMO pour aider à la santé osseuse alors qu’il a un effet antagoniste sur les récepteurs oestrogéniques dans les tissus du sein et de l’utérus.
L’efficacité de Femarelle® s’est avérée être similaire à l’efficacité de l’hormonothérapie, mais en raison de ses propriétés sélectives, Femarelle® fournit une solution plus sécuritaire pour la prise en charge à long terme de la ménopause.19
Femarelle® est donc, pour toutes ces raisons, une thérapie de première ligne appropriée, sécuritaire et efficace pour le traitement des symptômes de la ménopause et pour soutenir la santé osseuse.
Références
- Writing Group for the Women’s Health Initiative Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results from the Women’s Health Initiative randomized controlled trial. JAMA 2002; 288 (3): 321-33
- Million Women Study Collaborators: Breast cancer and hormone-replacement therapy in the Million Women Study. Lancet 2003; 362:419-27
- SOGC Clinical Practice Guideline, Managing Menopause. JOGC Sept 2014; Vol 36, no. 9
- Yoles I. et al. Efficacy and Safety of Standard versus Low Dose of Femarelle (Tofupill) for the Treatment of Menopausal Symptoms. J. of Clin Exper Obstet Gynecol 2004; 31(2):123-26.
- Genazzani AR et al. Brain region responsiveness to DT56a (Femarelle) administration on allopregnanolone and opioid content in ovariectomized rats. Menopause 2009; 16(5):1037-43.
- Nachtigal M. et al. A Prospective Study of DT56a (Femarelle) for the Treatment of Postmenopausal Vaginal Atrophy. Menopause book of abstract of the NAMS 22nd Annual Meeting, Sept, 2011, p. 55 (Article in process)
- Yoles I. et al. Tofupill/Femarelle (DT56a) - a New Phyto-Selective Estrogen Receptor Modulator-like Substance for the Treatment of Postmenopausal Bone Loss. Menopause 2003; 10(6):522-25
- Somjen D, Yoles I. DT56a (Tofupill/Femarelle), selectively stimulates creatine kinase specifc activity in skeletal tissues of rats but not in the uterus. J. of Steroid Biochemistry & Molecular Biology 2003; 86(1):93-98
- Somjen D. et al. DT56a (Femarelle/Tofupill) Stimulates Bone Formation in Female Rats. British J. of Obstetrics & Gynecology 2005; 112(7):981-85.
- Somjen D., Katzburg S. Lieberherr M., Hendel D., Yoles I. DT56a Stimulates Gender-Specifc Human Cultured Bone Cells In Vitro. J. of Steroid Biochemistry & Molecular Biology 2006; 98(1):90-96.
- Somjen D. et al. The Effects of Native and Synthetic Estrogenic Compounds as well as Vitamin D Less-Calcemic Analogs on Adipocytes Content in Rat Bone Marrow. J Endocrinol Invest. 2011;34(2):106-10
- Yoles I., and Lilling G. Pharmacological Doses of the Natural phyto-SERM DT56a (Femarelle) Have no Effect on MCF-7 Breast Cancer Cell-Line. European J. of Obstetrics & Gynecology & Reproductive Biology, 2006 ; 130(1):140-141.
- Nachtigall L. et al. Association of oral but not transdermal estrogen therapy with enhanced platelet reactivity in a subset of postmenopausal women. Menopause 2009;16(2):407-12
- Hoibraaten E, Abdelnoor M, Sandset PM. Hormone replacement therapy with estradiol and risk of venous thromboembolism--a population-based case-control study. Thromb Haemost 1999 Oct;82(4):1218-21.
- Nachtigall L., et al. The Selective Estrogen Receptor Modulator (SERM) DT56a (Femarelle), does not affect platelet reactivity in normal or thrombophilic menopausal women. Menopause 2011;18(3)285-288
- Somjen D. et al. DT56a (Femarelle); contrary to estradiol-17ß; is effective in human derived female osteoblasts in hyperglycemic condition. J Steroid Biochem Mol Biol. 2011; 123:25-29
- Oropeza M.V, Orozco S, Ponce H, Campos M.G. Tofupill lacks peripheral estrogen-like actions in the rat reproductive tract. Reproductive Toxicology 2005; 20(2):261-66. J. of Steroid Biochemistry & Molecular Biology
- Somjen D, Yoles I. DT56a (Femarelle): a Natural Selective Estrogen Receptor Modulator (SERM). J. of Steroid Biochemistry & Molecular Biology 2007; 104:252-58.
- Labos G., Trakakis E. et al Effcacy and safety of DT56a (Femarelle) compared to hormone therapy in Greek postmenopausal women. J. Endocrinol. Invest. 2013; 36(7):521-6
- Données au dossier : POMMSIS (Post Marketing Menopausal Symptoms International Survey)
- Dunnwald LK, Rossing MA, Li CI. Hormone receptor status, tumor characteristics, and prognosis: a prospective cohort of breast cancer patients. Breast Cancer Research 2007; 9(1):R6